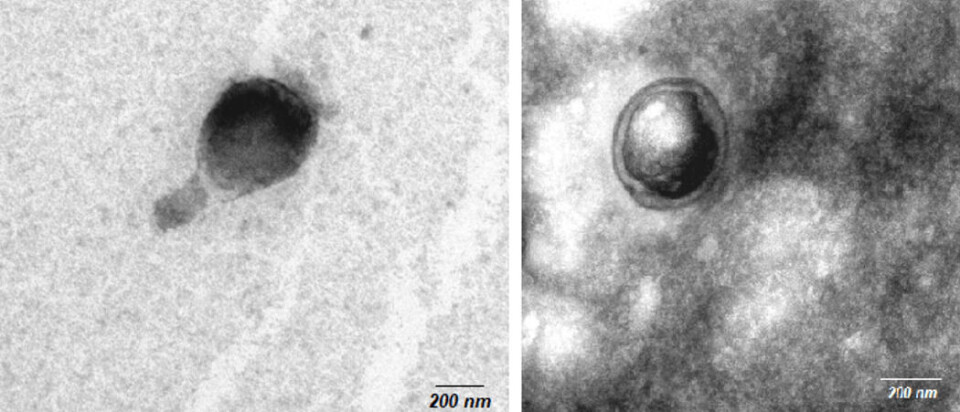
Vesículas producidas por Renibacterium podrían utilizarse para generar vacunas
Chile: Expertos creen que vesículas extracelulares producidas por el patógeno bacteriano podrían generar nuevas vacunas o ser estimulantes del sistema inmune del pez como un adyuvante natural.
En una reciente publicación, científicos chilenos descubrieron que R. salmoninarum produce Vesículas Extracelulares (VE) que contenían las proteínas p22 y p57, entre otros compuestos, y que además, poseían un efecto citotóxico in vitro en células de salmón.
¿Cuáles podrían ser las implicancias e importancia de estos resultados para la salmonicultura nacional? Para ello, primero habría que entender las funciones de estas proteínas.
Nuevos blancos de control o prevención
El Dr. Ruben Avendaño, investigador de la Universidad Andrés Bello (UNAB) y del Centro Incar, quien participó en el estudio, explica que la proteína p57, corresponde a una proteína de 57 kDa considerada el principal factor de virulencia de R. salmoninarum, que se encuentra abundantemente en la superficie celular de este patógeno y es parte de su antígeno más dominante.
“Distintos estudios demuestran y comprueban que participan en la patogenicidad de R. salmoninarum, siendo incluso liberada por la bacteria al ambiente externo en el pez. Además, se ha demostrado que otorga propiedades de hidrofobicidad y adherencia, capacidad de unirse a los eritrocitos del pez, aglutinar compuestos hemo, entre otras funciones”, señala el Dr. Avendaño.
En el caso de P22, el experto de la UNAB esclarece que también se asocia a características de hidrofobicidad debido a su alto grado de insolubilidad, “lo que significa que la bacteria no puede mantenerse expuesta al agua sino a protegerse de ella al interior de la célula, como sabemos que actualmente de este patógeno intracelular”.
“Estudios previos realizados por nuestro equipo en el 2017, demostraron que aislados chilenos sobreexpresan p22 en condiciones limitantes de hierro, lo que podría sugerir que R. salmoninarum produce más proteínas en condiciones estresantes. De hecho, demostramos que estas vesículas producidas por el aislado R. salmoninarum H-2 provocan infección en las líneas celulares testadas en el estudio, por lo que claramente estarían relacionadas con la patogenicidad de esta bacteria”, sostiene el experto.
En la publicación científica, también se describen otras proteínas desconocidas al interior de las VE con un peso molecular los 40 y 30-kDa. Sin embargo, el investigador del Centro Incar informa que mediante un estudio proteómico posterior pudieron identificar cada una de estas proteínas y no sólo de las vesículas sino de la bacteria, “lo cual es muy interesante y podrían ser nuevos blancos de control o prevención”.
Generación de vacunas
En cuanto a cómo estarían involucradas las VE en el efecto citotóxico celular de la bacteria, la Dra(c). Macarena Echeverría, otro de los autores del estudio, indica que se requieren experimentos adicionales idealmente in vivo para dilucidar esa interrogante, no obstante, se puede inferir algún rol de estas VE.
“Con nuestros resultados, podemos inferir que el rol de las VE en la infección de R. salmoninarum es temprano (ocurre durante las primeras 48 horas) y tóxico con concentraciones inferiores a 20 ug/mL. De igual manera, podrían haber otros mecanismos involucrados que se describan en los resultados proteómicos, pero lo más importante por ahora es evaluar el potencial de las vesículas en los propios peces”, sostiene Echeverría.
Finalmente, sobre las aplicaciones prácticas de estos resultados, la experta plantea que la principal aplicación podría ser la generación de vacunas, no sólo a nivel de producir grandes concentraciones de VE, lo que podría ser complejo operativamente, sino que igualmente se podría usarlas para estimular el sistema inmune del pez como un adyuvante natural para la aplicación de componentes de interés.
“De hecho, se han probado prototipos de vacunas que utilizan vesículas en patógenos Gram negativos que afectan especies de interés acuícola como Piscirickettsia salmonis Francisella noatunensis y Edwardsiella tarda, estimulando el sistema inmune y disminuyendo la mortalidad en peces posterior a la infección con el patógeno”, concluye la investigadora.




















